Awal budidaya laut atau marikultur di Indonesia ditandai dengan adanya keberhasilan budidaya mutiara oleh perusahaan Jepang pada tahun 1928 di Buton- Sulawesi Tenggara. Selanjutnya, awal tahun 1970-an dilakukan percobaan dan pengembangan budidaya rumput laut (Euchema sp.) di Pulau Samaringa-Sulawesi Tengah, dengan adanya kerjasama antara Lembaga Penelitian Perikanan Laut dan perusaan Denmark. Sementara itu, awal tahun 1980-an banyak pengusaha ekspor ikan kerapu hidup di Kepulauan Riau membuat karamba jaring tancap serta karamba jaring apung sebagai tempat penampungan ikan kerapu hidup hasil tangkapan sebelum di ekspor ke Singapura dan Hongkong. Adapun perkembangan budidaya laut khususnya dalam karamba jaring apung (KJA) dipicu oleh keberhasilan pembenihan ikan bandeng dan ikan kerapu di hatchery secara massal pada tahun 1990-an di Loka Penelitian Budidaya Pantai di Gondol Bali.
Mengapa?
Banyak sekali tujuan yang menjadi target pencapaian dalam pelaksanaan budidaya laut, diantaranya adalah:
- Efektif dan efisien
- Menghasilkan komoditas yang lebih baik dari segi kualitas maupun kuantitas.
Dengan adanya metode budidaya yang sesuai terhadap suatu jenis komoditas laut, diharapkan bisa merubah komoditas tersebut baik dari segi kualitas maupun kuantitas jika dibandingkan dengan komoditas lain yang sama yang hidup bebas di alam
- Potensi
- Memberdayakan masyarakat
- Menjaga kelestarian ekosistem di alam
PRINSIP DASAR BUDIDAYA LAUT
Kegiatan budidaya laut pada dasarnya sama dengan budidaya perikanan darat. Budidaya laut merupakan kegiatan yang baru di dunia perikanan. Beberapa alasan budidaya laut bisa berkembang, diantaranya sumber day aikan yang ditangkap sudah menurun sehingga nelayan beralih ke budidaya, budidaya perikanan di darat banyak menglami hambatan dan harga atau nilai jual komoditas budidaya laut relatif lebih tinggi dibanding dengan budidaya air tawar.
- A. Pemilihan Jenis Komoditas
Ada bebereapa aspek yang perlu dipertimbangkan dalam penentuan pilihan b iota laut yang akan dibudidayakan, diantaranya aspek permintaan pasar, pasok benih, sediaan teknologi budidaya, sediaan lahan, dan kemungkinan timbulnya dampak negatif terhadap lingkungan. Per timbangan untuk memilih komodit as laut yang akan dibudidayakan :
- Sebaikknya mengembangkan spesies asli/ lokal daripada introduksi atau impor.
- Memilih spesies yang sesuai dengan permintaan pasar.
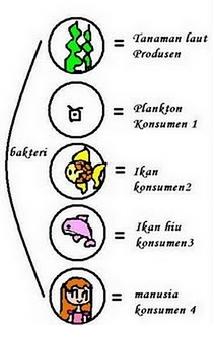
- Diversifikasi spesies budidaya diprioritaskan pada ikan pemakan plankton dan ikan herbivora. Jumlahnya lebih banyak daripada ikan karnivora.
- Jenis ikan pelagis lebih mudah dibudidayakan dilihat dari penerapan teknologinya dibandingkan dengan ikan demersal.
- Ikan yang tidak hanya bisa bernafas dengan insang atau ikan yang mempunyai labirin lebih mudah pemeliharaan dan tidak memerlukan mutu air yang baik.
- Ikan yang teknologi pembenihannya sudah maju sehingga pasokan benih baik jumlah dan kualitasnya tersedia setiap saat.
- Seluruh siklus hidup ikan budidaya harus dapat dikontrol dan teknologinya sudah dikuasai.
Banyak jenis biota laut yang sudah biasa dibudidayakan, seperti jenis ikan, krustasea, moluska, echinodermata, dan rumput laut. Ikan yang sudah biasa dibudidayakan adalah :
- Kerapu bebek
- Kerapu macan
- Kerapu lumpur
- Kakap merah
- Baronang
- Nila merah
- Bandeng
- Cobia
- Kerapu sunu
- Dan lain-lain
Jenis udang yang biasa dibudidayakan antara lain :
- Udang windu
- Udang barong
Sedangkan jenis-jenis moluska yang senantiasa dibudidayakan antara lain :
- Tiram daging
- Tiram mutiara
- Kerang hijau
- Kerang darah
- Kerang abalon
- Tiram mabe
- Dan lain-lain
- B. Pemilihan Lokasi
Sebagai langkah awal budidaya laut adalah pemilihan lokasi budidaya yang tepat. Oleh karena itu, pemilihan dan penentuan lokasi budidaya harus didasarkan pertimbangan ekologis, teknis, higienis, sosio-ekonomis, dan ketentuan peraturan perundang-undangan yang berlaku. Pemilihan lokasi sebaiknya dilakukan dengan mempertimbangkan gabungan beberapa faktor yang dikaji secara menyeluruh.
- 1. Persyaratan teknis
Sesuai dengan sifatnya yang sangat dipengaruhi oleh kondisi perairan, lingkungan bagi kegiatan budidaya laut dalam keramba jaring apung sangat menentukan keberhasilan usaha. Pemilihan lokasi yang baik harus memperhatikan aspek fisika, biologi, dan kimia perairan yang cocok untuk biota laut. Selain itu, pemilihan lokasi perlu juga mempertimbangkan aspek efisiensi biaya operasional budidaya.
- 2. Persyaratan sosial-ekonomi
Berikut beberapa aspek sosio ekonomi yang perlu mendapat perhatian dalam pemilihan dan penentuan lokasi.
a) Keterjangkauan lokasi. Lokasi budidaya yang dipilih sebaiknya adalah lokasi yang mudah dijangkau.
b) Tenaga kerja. Tenaga kerja sebaiknya dipilih yang memiliki tempat tinggal berdekatan dengan lokasi budidaya, terutama pemberdayaan masyarakat dan nelayan.
c) Sarana dan pra sarana. Lokasi budidaya sebaiknya berdekatan dengan sarana dan prasarana perhubungan ynag memadai untuk mempermudah pengangkutan bahan, benih, hasil dan lain-lain.
d) Kondisi masyarakat. Kondisi masyarakat yang lebih kondusif akan memungkinkan perkembangan usaha budidaya laut di daerah tersebut.
- 3. Persyaratan non-teknis
Persyaratan non-teknis yang harus dipenuhi dalam pemilihan lokasi adalah :
a) Keterlindungan. Lokasi budidaya harus terlindung dari bahaya fisik yang dapat merusaknya. Misalnya gelombang besar dan angin. Oleh karena itu, lokasi budidaya biasanya dipilih di tempat yang terlindung atau terhalang oleh pulau.
b) Keamanan lokasi. Masalah pencurian harus dipertimbangkan dalam pemilihan lokasi budidaya agar proses budidaya aman dan tidak terganggu.
c) Konflik kepentingan. Lokasi budidaya tidak boleh menimbulkan konflik kepentingan, misalnya, antara kegiatan perikanan dan nonperikanan (pariwisata).
d) Aspek peraturan dan perundang-undangan. Pemilihan lokasi harus sesuai dan tidak melanggar peraturan agar budidaya dapat berkelanjutan.
- C. Teknis Budidaya
Berbeda dengan budidaya air tawar, komoditas budidaya laut cukup banyak. Selain itu, metode atau teknologi budidaya laut lebih beragam, mulai dari pemanfaatan lahan dasar, penggunaan jaring atau rak tancap ( pen Culture ), Keramba Jaring apung.
a) Jaring Tancap
Jaring tancap ( pen Culture ) biasanya dipasang di bawah ( kolong ) rumah nelayan di pinggir pantai atau dipasang di tengah laut pada kedalaman 2-8 meter waktu surut terendah. Jaring tancap merupakan jaring kantong berbentuk persegi yang dipasang pada kerangka bambu atau kayu yang ditancap pada dasar perairan. Pasangan kayu / bambu ditancap rapat, seperti pagar, atau hanya dipasang di bagian sudut kantong jaring. Jaring sebagai lapisan dalam diikatkan pada kayu.
b) Keramba jaring apung
Keramba Jaring Apung ( KJA ) dapat dibuat dalam berbagai ukuran. Desain dan bahan tergantung pada kemudahan penanganan, daya tahan bahan baku,harga, dan faktor lainnya. Jaring atau wadah untuk pemeliharaan ikan di laut dibuat dari bahan polietilen. Bentuk dan ukuran bervariasi dan sangat dipengaruhi oleh jenis ikan yang dibudidayakan, ukuran ikan, kedalaman perairan, serta faktor kemudahan dalam pengelolaan.
BUDIDAYA RUMPUT LAUT
Rumput laut merupakan sumber utama penghasil agar-agar, alginat dan karaginan yang banyak dimanfaatkan dalam industri makanan, kosmetik, farmasi dan industri lainnya, seperti industri kertas, tekstil, fotografi, pasta dan pengelengan ikan.
Beberapa jenis rumput laut yang telah berhasil di budidayakan dan telah berkembang dengan baik di tingkat pembudidaya adalah Kappaphycus alvarezii dan euchema denticulatum yang di pelihara di perairan pantai (laut).
- A. Pemilihan lokasi budidaya
Pertumbuhan rumput laut ditentukan oleh kondisi perairan sehingga kondisi rumput laut cenderung bervariasi dari lokasi budidaya yang berbeda.
Karakteristik ekologi suatu lokasi merupakan salah satu faktor yang dapat mempengaruhi keberhasilan usaha rumput laut. Parameter yang perku di oerhatikan adalah sebagai berikut:
- Arus
Rumput laut merupakan tanaman yang memperoleh makanan (unsur hara) melalui aliran air yg melewatinya. Kecepatan arus yang baik untuk budidaya adalah 20-40 cm/detik.
- Dasar Perairan
Dasar perairan berupa pecahan karang dan pasir karang merupakan kondisi dasar perairan yang sesuai dengan budidaya rumput laut.
- Kedalaman
Kealaman perairan sangat tergantung dengan metode budidaya yang akan di pilih. Pemilihan kedalaman perairan yang tepat dilakukan untuk manghindari kekeringan dan mengoptimalkan pencapaian sinar matahari ke rumput laut.
- Kadar Garam
Kadar garam yang sesuai untuk pertumbuhan rumput laut berkisar antara 28-35 g/Kg
- Kecerahan
Lokasi budidaya rumput laut sebaiknya pada perairan yang jernih dengen tingkat kecerahan yang tinggi.
- Ketersediaan bibit
Bibit rumput laut yang berkualitas sebaiknya tersedia di sekitar lokasi budidaya yang di pilih, baik yang bersumber dari alam maupun dari budidaya sendiri.
- Orgaisme Pengganggu
Lokasi budidaya diusahakan pada lokasi yang tidak banyak terdapat organisme pengganggu, seperti ikan baronang, bintang laut, bulu babi, dan penyu.
- B. Metode Budidaya
- Metode Lepas Dasar
Metode ini dilakukan di atas dasar perairan yang berpasir atau pasir berlumpur dan tyerlindung dari hempasan gelombang yang besar. Hal ini penting untuk memudahkan pamasagan patok . biasanya lokasi dikelilingi oleh karang pemecah gelombang. Selain itu, sebaiknya memiliki kedalaman air sekitar 50cm pd surut terendah dan 3m pada saat pasang tertinggi.
- Metode Rakit Apung
Merupakan budidaya rumput laut dengan cara mengikat rumput laut pada tali ris. Yang diikat pada rakit apung yang terbuat dari bambu. Satu unit rakit apung berukuran 2,5 m – 5 m. Tanaman harus selalu berada sekitar 30-50 cm dibawah permukaan air laut.
- Metode Rawai
Metode ini dikenal dengan metode long line yang menggunakan tali panjang yang di bentangkan. Metode ini merupakan salah satu metode permukaan yang paling banyak di minati pembudidaya. Alat dan bahan yang digunakan dalam metode ini lebih tahan lama, relatif murah, dan mudah diperoleh.
- Metode Jalur
Metode ini merupakan kombinasi antara metode rakit dengan rawai. Kerangka metode ini ternuat dari rakit (bambu) yang tersusun sejajar. Kedua ujung setiap bambu dihubungkan dengan tali utama berdiameter 6mm sehingga membentuk persegi panjang dengan ukuran 5m – 7m per petak dengan satu unit terdiri dari 7-10 petak.
Pada kedua ujung setiap unit di beri jangkar penanaman dimulai dengan mengikat bibit rumput laut ke tali jalur. Tali tersebut telah di lengkapi dengan tali polietilen berdiameter 0,2c sebagai pengikat bibit. Adapun jaraknya sekotar 25cm.
- C. Pengolahan budidaya
- 1. Penyediaan bibit
Penyediaan bibit rumput laut diambil dari alam, budidaya, dan pembenihan. Budidaya rumput laut dapat mengambbil benih dari alam bila lokasi budidaya tersebut memiliki potensi bibit alam.
- 2. Penanganan bibit selama pengangkutan
Pengangkutan bibit selama pengangkutan dari tempat asal ke lokasi budidaya dilakukan sebagai berikut :
- Bibit harus dijaga agar tetap lembab
- Usahakan agar tidak terkena air tawar, hujan, embun, mminyak, dan kotoran lainnya karena akan merusak bibit.
- Bibit tidak boleh terkena sinar matahri
- Bibit diletakkan pada daerah yang jahu dari sumber panas, seperti mesin mobil atau perahu.
- 3. Penanaman bibit
Bibit yang akan ditanam dipilih yang berkualitas. Kepadatan penanaman bibit rumput laut tergantung dari jenis dan metode budidaya yang akan digunakan. Untuk budidaya Euchema sp. Bobot bibit yang digunakan sekitar 50-100 ggr per ikatan dengan jarak tidak kurang dari 25 cm.
- 4. Perawatan tanaman
Agar budidaya dapat dilakukan dengan baik dan berhasil maka harus dilakukan perawatan dan pemeliharaan. Perawatan bukan hanya pada tanaman itu sendiri tetapi juga pada alat-alat dan perangkat budidaya. Oleh karena itu, pengelola rumput laut sangat diperlukan untuk memperkecil kemungkinan kerusakan tanaman.
Kegiatan perawatan meliputi pembersihan lumpur, kotoran, dan biofouling yang menempel pada thallus rumput laut; penyisipan tanaman yang rusak atau lepas dari ikatan; penggantian patok, pelampung dan lain-lain.
- D. Pengendalian Hama dan Penyakit
Hama tanaman pada budidaya rumput laut umumnya merupakan organisme laut, terutama ikan baronang dan penyu yang memangsa tanaman. Secara alami, organisme tersebut hidup dengan rumput laut sebagai makanan utamanya. Hama tersebut dapat menimbulkan kerusakan fisik pada tanaman budidaya.
Penyakit ice-ice merupakan kendala utama budidaya rumput laut. Gejala ini dikenal juga dengan nama white spot. Rumput laut yang terserang penyakit itu antara lain pertumbuhan yang lambat, terjadinya perubahan warna thallus menjadi pucat atau warna tidak cerah, dan sebagian atau seluruh thallus pada beberapa cabang mengalami keputihan serta membusuk. Penyakit tersebut terutama disebabkan oleh perubahan lingkungan, seperti arus, suhu, dan kecerahan. Kecerahan air yang sangat tinggi dan rendahnya kelarutan unsur hara nitrat dalam perairan juga merupakan penyebab munculnya penyakit tersebut.
- E. Panen
Waktu panen sangat ditentukan oleh waktu tanaman dalam mencapai tingkat kandungan bahan utama maksimal. Dengan demikian panen rumput laut sebaiknya dilakukan setelah mencapai pemeliharaan selama 45 hari. Namun, panen untuk rumput laut untuk bibit dilakukan pada saat umur tanaman berkisar 25-35 hari.
Panen dilakukan pada cuaca yang cerah agar kualitas rumput laut yang dihasilkan terjamin. Panen dapat dilakukan dengan dua cara yaitu ; panen selektif atau parsial dan secara keseluruhan. Panen secara selektif dilakukan dengan cara memotong tanaman secara langsung tanpa melepas ikatan dari tali ris. Keuntungan cara ini adalah penghematan tali rafia pengikat rumput laut, tetapi memerlukan waktu yang agak lama. Sementara itu panen kaseluruhan dilakukan dengan mengangkut seluruh tanaman sekaligus sehingga waktu kerja yang diperlukan lebih singkat.
Panen rumput laut secara keseluruhan pada metode lepas dasar, rakit apung, rawai, dan jalur dilakukan dengan cara berikut :
- Rumput laut dibersihkan dari kotoran atau tanaman lain yang melekat sebelum dipanen.
- Tali ris yang penuh dengan ikatan rumput laut dilepaskan dari bambu atau tali utama.
- Gulungan dari tali ris yang berisi ikatan rumput laut diletakan di sampan atau wadah transportasi lainnya.
Diusun Oleh
Gusti Septiandina 230210080002
Reza Muhammad Azhar 230210080007
Jimy Kalther 230210080049
Enjang Hernandi Hidayat 230210080068
Alfian Nurrachman 230210080071
Andy Catur 2302100700
Marine Culture
Ilmu Kelautan UNPAD 2010